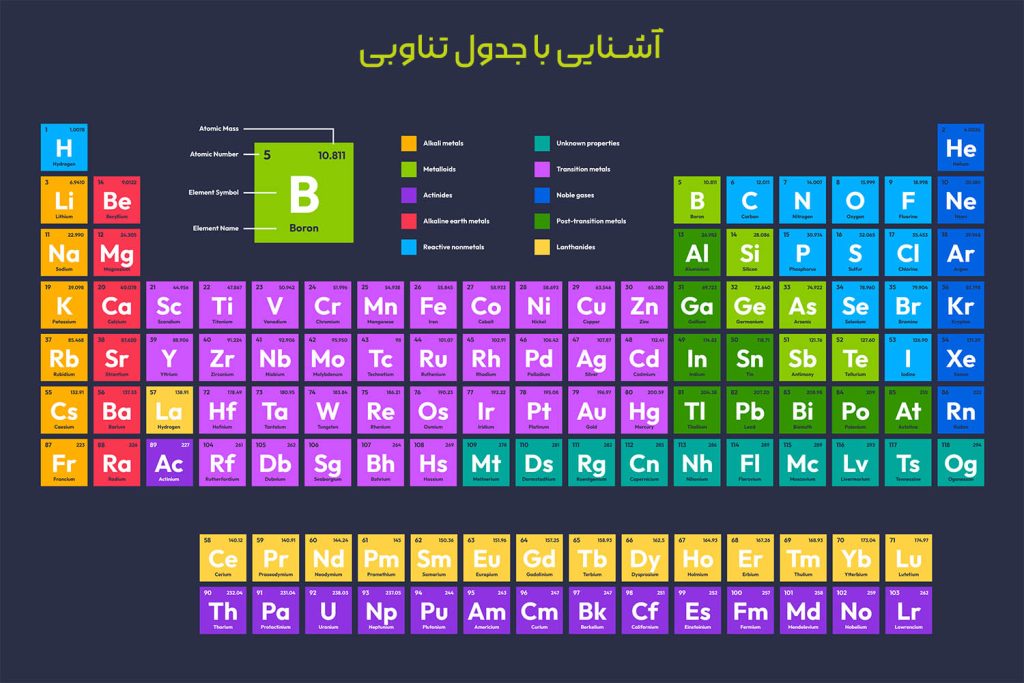
جدول تناوبی
تا سال ۲۰۱۵تعداد عناصر شیمیایی 118 عنصر بوده است که ۱۱۴ عنصر به صورت رسمی از سوی اتحادیه بینالمللی شیمی محض و کاربردی پذیرفته شده و به ثبت رسیده اند . از بین این 118 عناصر ، 98 عنصر در طبیعت یافت گردیده است از بین 98 عنر یافت شده نیز 84 عنصرهای پایدار یا دارای نیمعمر بیش از سن زمین هستند . این عناصر در جدولی به نام جدول تناوبی یا جدول عناصر شیمیایی که به آن جدول مندلیف هم میگویند گردآوری شده است .

جدول تناوبی چیست ؟
جدول تناوبی عنصرهای شیمیایی در واقع لیستی از تمام عناصر موجود شناخته شده در طبیعت همراه با آرایش الکترونیکی ، پایه عدد اتمی و ویژگی های شیمیایی میباشد . ترتیب عدد اتمی در جدول تناوبی یا به اصلاح جدول مندلیف از اتم پایین به بالا میباشد . شکل و ساختار حدول عناصر شیمیایی به صورت مستطیل است . اگر بخواهیم جدول مندلیف را به بخش های مختلف تقسیم کنیم 4 بخش اصلی دارد .
- مستظیل سمت چپ بخش s
- مستطیل راست بخش p
- مستطیل میانه بخش d
- مستطیل پایین بخش f

لیست قیمت لوله استیل 304 و 316
ظاهر جدول تناوبی
نماد عنصرهای شیمیایی بخش اصلی بخش اصلی همه نسخه های جدول عناصر شیمیایی است وو ترکیب و یا ذره اتمی در آن وجود ندارند . هر یک عدد اتمی یکتا برای هر عنصر شیمیایی وجود دارد . این عدد نشانگر شمار پروتونها در هستهٔ اتم آن عنصر میباشد . شمار نوتورهای هر عنصر میتواند متفاوت باشد . این حالت ایزوتوپ نام دارد .
برخی از قوانین جدول تناوبی
- دوره ها به صورت افقی در داخل جدول در ردیف ها حرکت می کنند
- و با حرکت از چپ به راست ، عدد اتمی یکی بالا می رود.
- عدد اتمی تعداد پروتونهای موجود در یک اتم است.
- حداقل عدد اتمی 1برای عنصر هیدروژن و بیشترین آنها 118 متعلق به عنصر اوگانسون میباشد
نمونه حالت ایزوتوپ در عناصر
برای نمونه ، کربن از 3 ایزوتوپ طبیعی برخوردار است . همهٔ ایزوتوپهای کربن ۶ پروتون، و بیشتر آنها ۶نیز از 6 نوترون برخوردار است ؛ اما حدود 1 درصد از آنها 7 نوترو داشته و همچنین درصد بسیار کمی نیز 8 نوترو دارد . ایزوتوپ ها در جدول مندلیف جدا درج نمیشود و عددی میانگین نیزبه عنوان عدد جرم اتمی در نظر گرفته میشود . در برخی عناصر نیز عدد جرم اتمی در جدول تناوبی داخل پرانتز قرار میگیرد جرا که هیچ ایزوتوپ پایداری ندارند .
قیمت ورق استیل 304 و 316
دستهبندی جدول تناوبی
عنصرها در جدول مندلیف در 7 ردیف و 18 ستون چیده شده اند . همچنین عنصرها در دستهبندی دیگری بر اساس لایهٔ الکترونی f,d,p,s چیده میشوند . هر ستون یا بهتر از بگوییم هر ستون عمودی یک خانواده بشمار میرود .
آرایش الکترونی در جدول تناوبی
الکترونها در هر عنصر، مجموعهای از لایههای الکترونی را پُر میکند. هر چه عدد اتمی یک عنصر افزایش یابد، زیر لایه ها و لایه های بیشتری در آن به وحود می آید . این لایهها بر پایهٔ اصل آفبا یا قانون تراز انرژی پر میشوند . هر لایهٔ الکترونی از یک یا چند زیرلایه نشکیل شدهاست که به آنها لایههای s و p و d و f و g گفته میشود. برای نمونه، آرایش الکترونی نئون با عدد اتمی ۱۰ عبارت است از: 1s2 2s2 2p6 که دو الکترون در لایهٔ نخست و هشت الکترون در لایهٔ دوم (دو تا در زیرلایهٔ s و شش تا در زیرلایهٔ p) جای میگیرد. برای نمونه، فلزهای قلیایی و عنصر هیدروژن، تنها از یک لایه الکترون در لایه s برخوردارند . آرایش الکترونی عنصرهای جدول، الگویی تکرار شونده دارند.
شعاع اتمی در جدول تناوبی
توانایی اندازه گیری شعاع یک اتم به صورت محزا وحود ندارد ، ولی میتوان با اندازهگیری فاصلهٔ میان هستههای دو اتم که با هم پیوند دارند،شعشع اتمی یک اتم را محاسبه کرد .به عنوان نمونه ، وقتی که دو اتم در یک عنصر با یکدیگر پیوندی دارند ، شعاع اتمی هر یک از آنها نصف طول پیوند دو اتم میباشد که این اندازه گیری و محاسبه هم دقیق و هم شدنی است . هرچند که این مقدار در پیوندهای مختلف، اندکی متفاوت است؛ اما برای یک میانگین شعاع اتمی میتوان در نظر گرفت. این تغییر شعاع اتمی و در کنار آن تغییر در ویژگیهای فیزیکی و شیمیایی عنصرها را میتوان با کمک نظریههای اتمی دربارهٔ لایههای الکترونی توضیح داد. بهطور کلی، با حرکت به سمت چپ و پایین جدول عناصر شیمیایی نیز عدد شعاع اتمی نیز بیشتر میشود . این فرمول های به دست آمده صحت فیزیک کوانتوم را به ما ثابت میکند .
انرژی یونش در جدول تناوبی
نخستین انرژی یونش
از یک اتم خنثی در حالت گازی انرژی لازم برای جدا کردن سستترین الکترون ، نخستین انرژی یونش میباشد .
دومین انرژی یونش
دومین انرژی یونش، انرژی مورد نیاز برای جدا کردن دومین الکترون از یک اتم است.
انرژی یونش در مراتب بالاتر
انرژیهای یونش رده های بالاتر نیز به همین ترتیب تعریف میشوند . برای یک اتم مشخص، با افزایش درجهٔ یونش،انرژی یونش نیز بیشتر میشود . بر الکترونهای لایههای نزدیکتر به هسته، نیروی جاذبهٔ الکترواستاتیک بیشتری اعمال میشود؛ پس انرژی مورد نیاز برای حداسازی آنها نیز افزوده میگردد . با حرکت به بالا و سمت راست نیز انرژی یونش بیشتر میگردد .
در هر سیکل جدول ، با دو پرش بزرگ روبرو خواهید شد یک پرش در گذر از گاز نجیب به فلز قلیایی بعدی بوده و پرش دوم که کوچکتر میباشد پیش از گروه ۱۳ رخ میدهد.هنگامی که همهٔ الکترونهای یک لایه جدا میگردند انرژی یونش بعدی به شدت افزایش مییابد . در هر دو حالت، ابتدا آخرین لایهٔ آرایش الکترونی پر شده و سپس الکترون بعدی در لایهٔ جدید قرار میگیرد؛ بنابراین انرژی مورد نیاز برای جداسازی آن بسیار کمتر خواهد شد . چنین رخدادی در انرژیهای یونش متوالی یک عنصر نیزدیده میشود.
الکترونگاتیوی در جدول تناوبی
گرایش یک اتم به جذب الکترون را الکترونگاتیوی میگویند که وابسته به دو عامل عدد اتمی و فاصلهٔ الکترونهای لایهٔ آخر آن اتم با هسته است .لینوس پاولینگ این پیشنهد را در سال 1932 عنوان کرد . افزایش الکترونگاتیوی به سمت بالا و سمت راست جدول صورت میگیرد .فلوئور و سزیم کمترین الکترونگاتیوی را در میان عنصرهای شناخته شده طبیعت دارند .
استثناهایی در تغییرات تناوبی الکترونگاتیوی مشاهده میشوند. الکترونگاتیوی عنصرهای گروه ۱۳ و ۱۴ در دورهٔ چهارم بیشتر از دورهٔ سوم است که دلیل آن، پر شدن لایهٔ d (که درونیتر است) و کمتر شدن شعاع اتمی است. استثنای دیگر، بالا بودن غیرعادی الکترونگاتیوی سرب در مقایسه با عنصرهای پیرامونش است که به نظر میرسد به دلیل اشکال در تحلیل دادهها باشد.[۳۴] روشهای محاسباتی دیگر، متفاوت با آنچه مورد استفاده پاولینگ بوده، نشان میدهند که این عنصرها دارای رفتار دورهای طبیعی هستند.
الکترونخواهی در جدول تناوبی
تنها الکترونخواهی فلزات قلیایی خاکی (گروه ۲)، گروههای ۷ و ۱۲ و گازهای نجیب (گروه ۱۸) مثبت است. زمانی که واکنش افزوده شدن یک الکترون به اتم در حالت گاز و تبدیل اتم خنثی به یون منفی صورت میگیرد الکترون خواهی میباشد که برای بیشتر عنصرها، این فرایند با آزاد شدن انرژی همراه بوده و در نتیجه، مقدار الکترونخواهی برای اولین الکترون، مقدار منفی بشمار میرود . (در واقع، برای این عنصرها مقدار تجربی الکترونخواهی اندازهگیری نشدهاست) دلیل این رخداد، پر بودن (مانند گروه ۲، ۱۲ و ۱۸) یا نیمهپر بودن آخرین لایهٔ آرایش الکترونی این عنصرها (مانند گروه ۷) است. در هر دوره، بیشترین الکترونخواهی منفی مربوط به گروه هالوژنها است. کلر بیشترین مقدار الکترونخواهی را در میان عنصرهای جدول تناوبی دارد . الکترونخواهی عنصرهای گروه ۱۵ نیز به دلیل نیمهپر بودن لایهٔ p کمتر از گروههای مجاور است.
جدول مندلیف چیست ؟
در سالهای 1969 و 1970 دو تن به ساخت جدول عناصر شیمیایی به صورت مستقل پرداختند .
استاد روس شیمی ،دیمیتری مندلیف
شیمیدان آلمانی، ژولیوس لوتار میر
نخستین نسخه از جدول عناصر شیمیایی را دیمیتری مندیل منتشر کرد . گرچه نسخه منتشر شده از جدول لوتار میر ، نسخه پیشرفته جدول مندلیف است ام حالا سوال اینجاست
چرا به جدول عناصر شیمیایی جدول مندلیف میگویند ؟
خب در رابطه با این دو شیمیدان باید گفت که هر دو نفر، عناصر را در ردیف و ستون ها نسبت به وزن اتمی جیده اند . ویژگی های عناصر به صورت مرتب در ابتدای هر ردیف و یا ستون عنوان میشد . اما دیمیتری مندلیف دو کا بسیار مهمی کرد که همین عمل موجب شد تا به جدول عناصر شیمیایی ، امروزه در مراکز آموزشی آن را جدول مندلیف هم میگویند . نخستین کار این بود که جای عناصر شناخته نشده را تعیین و خالی گذاشت . مندلیف جدول عناصر شیمیایی را به ترتیب وزن اتم دسته بندی کرده بود که بعدها متوجه شدند که او نا خواسته عناصر شیمیایی را نسبت به بار هسته مرتب کرده بود .
جدول تناوبی در قالب مثال
هر چه در روی این کره خاکی میبینید متشکل از عناصر شیمیایی میباشد . جدول عناصر شیمیایی به تنهایی یک تعریف دارد و در دنیای آزمایشگاهی یک تعریف دیگر . ما یک مثال را برای شما ذکر میکنیم . مثلا همه ما فرمول ترکیب شیمیایی آب را میدانیم . H۲O ترکیبات شیمیایی آب است که همین ترکیب شیمیایی بیش از 2/3 سطح کره زمین را فرا گرفت است . حال شما در آزمایشگاه ها میتوانید یک جس را برای آنالیز ببرید تا متخصصین به شما بگویند جسم مورد نظر شما از چه ترکیباتی تولید شده است . مثلا ما در جدول زیر یک لوله استیل 304 را آنالیز میکنیم . ترکیبات لوله استیل را ببینید . و یا حتی یک ورق استیل 316 را میتوانید در جدول بعدی مشاهده کنید . این اعداد و جداولی که شما میبینید درصد تشکیل دهنده هر عنصر و برخی معیارهای مرتبط با فرآیند ورق استیل را نشان میدهد
Ni | Cr | Mo | Mn | Si |
|---|---|---|---|---|
11.0 – 15.0 | 18.0 – 20.0 | 3.0 – 4.0 | 2.0 Max | .75 Max |
C | N | S | P | Fe |
0.03 Max | 0.1 Max | 0.03 Max | 0.045 Max | Balance |
گرید | C | Mn | Si | P | S | Cr | Mo | Ni | N | |
استیل 304 | min. max. | – 0.08 | – 2.0 | – 0.75 | – 0.045 | – 0.030 | 18.0 20.0 | – | 8.0 10.5 | – 0.10 |
سوالات رایج جدول تناوبی
عدد اتمی چیست ؟
تعداد پروتونهای موجود در هسته اتم را عدد اتمی میگویند .
آیا 118 عنصر شناخته شده در جدول مندلیف در طبیعت وجود دارند ؟
خیر . 94 عنصر موجود در طبیعت کشف شده و باقی عناصر در آزمایشگاه ساخته میشوند .از این تعداد عناصر جدول عناصر شیمیایی 84 عنصر پایدار میباشند و باقی عناصر نیز در فرآیند شکست سایر عناصر به وجود می آیند
شعاع اتمی را چگونه اندازه گیری میکنند ؟
نصف فاصله موجود در هسته دو اتم را شعاع اتمی مینامند که آن را در مولکولها اندازه گیری میکنند .
خاصیت فلزی اتم چیست ؟
مقدار تمایلی که اتم برای از دست دادن الکترون دارد را خاصیت فلز اتم میگویند .
فرق نقطه ذوب و نقطه جوش چیست ؟
در عدد گذاری نقطه جوش و نقطه ذوب در جدول تناوبی ، نقطه جوش یعنی زمانی که درجه حرارت عنصر تاجایی بالا رود که فشار بخار مایع با فشار اطراف یکسان گردد . اما در نقطه ذوب اشاره میشود به درجه ای از حرارت که عنصر از حالت جامد به حالت مایع تبدیل میشود .
عناصر شیمیایی جدول مندلیف از 61 تا 90
- پرومتیوم : عدد اتمی 61 و نماد شیمیایی pm
- ساماریوم : عدد اتمی 62 و نمادی شیمیایی sm
- یوروپیوم : عدد اتمی 63 و نماد شیمیایی eu
- گادولینیوم در جدول تناوبی : عدد اتمی 64 و نماد شیمیایی gd
- تربیوم : عدد اتمی 65 و نماد شیمیایی tb
- دیسپروزیوم : عدد اتمی 66 و نماد شیمیایی dy
- هولمیوم در جدول عناصر شیمیایی: عدد اتمی 67 و نماد شیمیایی ho
- اربیوم : عدد اتمی 68 و نماد شیمیایی er
- تولیوم در جدول مندلیف : عدد اتمی 69 و نماد شیمیایی tm
- ایتربیوم:عدد اتمی 70 و نماد شیمیایی yb
- لوتیتوم : عدد اتمی 71 ونماد شیمیایی lu
- هافنیوم : عدد اتمی 72 و نماد شیمیایی hf
- تانتال : عدد اتمی 73 و نماد شیمیایی ta
- تنگستن : عدد اتمی 74 و نماد شیمیایی w
- رنیوم ک عدد اتمی 75 و نماد شیمیایی re
- اسمیم : عدد اتمی 76 و نماد شیمیایی os
- ایریدیوم : عدد اتمی 77 و نماد شیمیایی ir
- پلاتین در جدول تناوبی : عدد اتمی 78 و نماد شیمیایی pt
- عنصر طلا : عدد اتمی 79 و نماد شیمیایی au
- جیوه : عدد اتمی 80 و نماد شیمیایی hg
- تالیوم : عدد اتمی 81 و نماد شیمیایی ti
- عنصر سرب در جدول تناوبی : عدد اتمی 82 و نماد شیمیایی pb
- بیسمون : عدد اتمی 83 و نماد شیمیایی bi
- پولونیوم : عدد اتمی 84 و نماد شیمیایی po
- استاتین : عدد اتمی 85 و نماد شیمیایی at
- رادون : عدد اتمی 86 و نماد شیمیایی rn
- فرانسیوم : عدد اتمی 87 و نماد شیمیایی fr
- رادیوم : عدد اتمی 88 و نماد شیمیایی ra
- آکتینیوم در جدول مندلیف : عدد اتمی 89 و نماد شیمیایی ac
- توریوم : عدد اتمی 90 و نماد شیمیایی th
لیست عناصرجدول تناوبی : از 91 تا 118
- پروتاکتینیوم : عدد اتمی 91 و نماد شیمیایی pa
- اورانیوم : عدد اتمی 92 و نماد شیمیایی u
- نپتونیوم : عدد اتمی 93 و نماد شیمیایی np
- پلوتونیوم : عدد اتمی 94 و نماد شیمیایی pu
- امریسیوم : عدد اتمی 95 و نماد شیمیایی am
- کوریوم : عدد اتمی 96 و نماد شیمیایی cm
- برکلیوم : عدد اتمی 97 و نماد شیمیایی bk
- کالیفرنیوم : عدد اتمی 98 و نماد شیمیایی cf
- اینشتینیوم : عدد اتمی 99 و نماد شیمیایی es
- فرمیوم : عدد اتمی 100 و نماد شیمیایی fm
- مندلیفیوم در جدول تناوبی : عدد اتمی 101 و نماد شیمیایی md
- نوبلیوم : عدد اتمی 102 و نماد شیمیایی no
- لارنسیوم : عدد اتمی 103 و نماد شیمیایی lr
- رادرفوردیوم : عدد اتمی 104 و نماد شیمیایی rf
- دوبنیوم : عدد اتمی 105 و نماد شیمیایی db
- سیبورگیوم : عدد اتمی 106 و نماد شیمیایی sg
- بوریم : عدد اتمی 107 و نماد شیمیایی bh
- هاسیم : عدد اتمی 108 نماد شیمیایی hs
- مایتنریوم : عدد اتمی 109 و نماد شیمیایی mt
- دامشتادیوم در جدول مندلیف : عدد اتمی 110 و نماد شیمیایی ds
- رونتگنیم : عدد اتمی 111 و نماد شیمیایی rg
- کوپرنیسیوم : عدد اتمی 112 و نماد شیمیایی cn
- نیهونیوم : عدد اتمی 113 و نماد شیمیایی nh
- فلروویوم : عدد اتمی 114 و نماد شیمیایی fl
- مسکوویم : عدد اتمی 115 و نماد شیمیایی mc
- لیرموریوم در جدول تناوبی : عدد اتمی 116 و نماد شیمیایی lv
- تنسین : عدد اتمی 117 و نماد شیمیایی ts
- اوگانسون : عدد اتمی 118 و نماد شیمیایی og
لیست عناصر جدول تناوبی 1 تا 30
- هیدروژن : عدد اتمی 1 و نماد شیمیایی H
- عنصر هلیوم : عدد اتمی 2 و نماد شیمیایی he
- عنصر لیتیوم : عدد اتمی 3 و نماد شیمیایی li
- بریلیوم : عدد اتمی 4 و نماد شیمیایی be
- بور : عدد اتمی 5 و نماد شیمیایی b
- کربن : عدد اتمی 6 و نماد شیمیایی c
- نیتروژن : عدد اتمی 7 و نماد شیمیایی n
- اکسیژن : عدد اتمی 8 و نماد شیمیایی o
- فلوئور : عدد اتمی 9 و نماد شیمیایی f
- نئون : عدد اتمی 10 و نماد شیمیایی ne
- عنصر سدیم : عدد اتمی 11 و نماد شیمیایی na
- عنصر منیزیم : عدد اتمی 12 و نماد شیمیایی mg
- آلومینیوم : عدد اتمی 13 و نماد شیمیایی al
- سیلیسیوم : عدد اتمی 14 و نماد شیمیایی si
- فسفر : عدد اتمی 15 و نماد شیمیایی p
- گوگرد در جدول عناصر شیمیایی : عدد اتمی 16 و نماد شیمیایی s
- کلر : عدد اتمی 17 و نماد شیمیایی cl
- آرگون : عدد اتمی 18 و نماد شیمیایی ar
- پتاسیم : عدد اتمی 19 و نماد شیمیایی k
- کلسیم : عدد اتمی 20 و نماد شیمیایی ca
- اسکاندیوم : عدد اتمی 21 و نماد شیمیایی sc
- تیتانیوم : عدد اتمی 22 و نماد شیمیایی ti
- وانادیوم : عدد اتمی 23 و نماد شیمیایی v
- عنصر کروم در جدول تناوبی : عدد اتمی 24 و نماد شیمیایی cr
- منگنز : عدد اتمی 25 و نماد شیمیایی mn
- آهن : عدد اتمی 26 و نماد شیمیایی fe
- عنصر کبالت : عدد اتمی 27 و نماد شیمیایی co
- نیکل : عدد اتمی 28 و نماد شیمیایی ni
- مس : عدد اتمی 29 و نماد شیمیایی cu
- روی : عدد اتمی 30 و نماد شیمیایی zn
لیست عناصر جدول تناوبی 31 تا 60
- گالیوم : عدد اتمی 31 و نماد شیمیایی ga
- ژرمانیوم : عدد اتمی 32 و نماد شیمیایی ge
- آرسنیک : عدد اتمی 33 و نمد شیمیایی as
- سلینم : عدد اتمی 34 و نماد شیمیایی se
- برم : عدد اتمی 35 و نماد شیمیایی br
- کریپتون : عدد اتمی 36 و نماد شیمیایی kr
- روبیدیوم : عدد اتمی 37 و نماد شیمیایی rb
- استرانسیوم : عدد اتمی 38 و نماد شیمیایی sr
- ایتریم : عدد اتمی 39 ونماد شیمیایی Y
- زیرکونیوم در جدول مندلیف : عدد اتمی 40 و نماد شیمیایی zr
- نیوبیوم : عدد اتمی 41 نماد شیمیایی nb
- عنصر مولیبدن : عدد اتمی 42 و نماد شیمیایی mo
- تکنسیوم : عدد اتمی 43 و نماد شیمیایی tc
- روتنیوم : عدد اتمی 44 و نماد شیمیایی ru
- رودیوم : عدد اتمی 45 و نماد شیمیایی rh
- پالادیوم : عدد اتمی 46 و نماد شیمیایی pd
- نقره : عدد اتمی 47 و نماد شیمیایی ag
- کادمیوم : عدد اتمی 48 و نماد شیمیایی cd
- ایندیوم : عدد اتمی 49 و نماد شیمیایی in
- قلع : عدد اتمی 50 و نماد شیمیایی sn
- آنتیموان : عدد اتمی 51 و نماد شیمیایی sb
- تلوریم : عدد اتمی 52 و نماد شیمیایی te
- عنصر ید : عدد اتمی 53 و نماد شیمیایی I
- زنون : عدد اتمی 54 و نماد شیمیایی xe
- سزیم با عدد اتمی 55 و نماد شیمیایی cs
- باریم : عدد اتمی 56 و نماد شیمیایی ba
- لانتان : عدد اتمی 57 و نماد شیمیایی la
- سریم در جدول تناوبی : عدد اتمی 58 و نماد شیمیایی ce
- پرازئودیمیوم : عدد اتمی 59 و نماد شیمیایی pr
- نئودیمیوم : عدد اتمی 60 و نماد شیمیایی nd
این برگه صرفا جهت مطالعه میباشد . کاربران عزیز و گرامی لطفا جهت فعالیت های آزمایشگاهی تماس حاصل نفرمایید . با تشکر استیل آرام
لذا دانشجویان عزیز میتوانید کلیه مقالات مرتبط با فلزات خود را برای بنده ارسال نمایید تا آنها را با ذکر نام نویسنده مقاله در سایت منتشر نماییم .




.
درود بر شما خیلی مطالبش مختصر و مفید بود ممنون از شما . اگه مطالب علمی دیگری هم در مورد فلزات داشتین حتما در سایت درج کنید ممنون راستی بنده درباره فولاد کربن و آستنیتی پستی پیدا نکردم . مرتبط با سایتتون میشه حتما بزارین
زنده باشید نظر لطفتونه
فولاد آستنیتی متریالهای مختلفی داره که در سایت میتونید کلیه محصولاتشو مطالعه کنید . اما چشم یک مقاله مفید و جامع در سایت قرار خواهیم داد . درباره فولاد کربن هم میتوانید روی لینک زیر کلیک کنید
https://steel-aram.ir/carbon-steel/
Visitor Rating: 5 Stars
خدا پدر ومادر شمارو بیامرزه وسعادتمند بشید
اتفاقی باصفحه تون برخورد کردم. خیلی عالی بود
بهترین توضیحی که برای جدول تا حالا دیدم. البته یه موردی هم داشت که بماند خدا توفیقتون بده
درود بر شما
ممنونم از دیدگاه خوبتون
سلام عزیز خدا قوت من یه معدن شن و ماسه رودخانه ای دارم تو ریز دانه ۱۰درصد fe2o3 ومقدار کمی منگنز منیزیم وتیتان داره میشه جدا کرد ممنون ضمنا اطلاعات عالی بود